¿Se puede crear vida artificial?
6 de agosto de 2024
"La evolución crea estructuras y patrones que con el tiempo son más complicados, con más conocimientos, más inteligencia, más creatividad, más capaz de expresar los sentimientos más elevados, como ser amorosos. Así que nos estamos moviendo en la misma dirección con la que se ha descrito a Dios, que dispone de estas cualidades sin límites. La evolución es un proceso espiritual y nos hace más divinos. Ray Kurzweil".
En la misma línea se pronuncia el libro «Homo Deus: Breve historia del mañana» de Yuval Noah Harari, cuando describe la forma en la que muchos de los avances científicos que ahora se están realizando nos acercan a una situación en la que el ser humano adquiere cualidades habitualmente atribuidas a los Dioses. Y la posibilidad de crear vida de forma artificial, es sin duda una de estas cualidades.
Desde que Friedrich Wöhler sintetizó una molécula de urea en 1928, las personas científicas no han parado de trabajar con la vista puesta en la creación de vida artificial y es por esto por lo que estamos muy cerca de poder afirmar que podemos hacer con la vida lo mismo que hemos hecho con los ordenadores, programarla. Para ello ha sido fundamental el descubrimiento de la estructura molecular del ADN, la capacidad para secuenciar el genoma de cualquier ser vivo y el desarrollo de tecnologías de edición genética como CRISPR. Todo esto ha permitido en los últimos años que el ser humano haya podido realizar desarrollos como la producción de alimentos transgénicos o la clonación de animales, pero la biología sintética va un paso más allá y es lo que queremos descubrir a lo largo de este artículo.
La Biología Sintética se puede definir como el diseño y fabricación de componentes y sistemas biológicos que no existen de forma normal en la naturaleza, así como las técnicas que permiten introducir modificaciones en los diseños de los sistemas biológicos ya existentes. Por lo tanto, su misión es la creación de nuevos organismos capaces de responder a determinados estímulos de una forma programada, controlada y fiable. Esto es posible mediante la introducción de secuencias de ADN que codifican nuevos genes, muy a menudo procedentes de otras especies distintas de aquella sobre la que se actúa, por ejemplo al trabajar con una célula bacteriana que es modificada genéticamente al añadirle genes extraños, ya sean de virus, de otras bacterias o de seres humanos. Estos nuevos genes y las nuevas regulaciones genéticas asociadas a ellos son capaces de inducir nuevos comportamientos en las células que los reciben, permitiendo su reprogramación. De esta forma, la biología sintética presenta una expectativa importante de utilización en actividades como el diseño de fármacos inteligentes, la terapia génica, la regeneración de tejidos, la biorremediación, los biosensores y la bioenergía.
Con el objetivo de potenciar esta nueva área de la ciencia se organizan iniciativas como IGEM, la competición sobre biología sintética promovida por el MIT. En esta competición las agrupaciones estudiantiles reciben en el comienzo del verano un kit de partes biológicas, procedente del Registry of Standard Biological Parts. Este kit consiste en una variedad de componentes genéticos tales como promotores, terminadores, reporteros y vectores de clonación. Los estudiantes trabajan en sus universidades o instituciones durante el verano, utilizando estas piezas y creando otras nuevas, con el objetivo de diseñar sus propios sistemas biológicos e implementarlos en células. A través de esta competición se pretende construir sistemas biológicos a partir de los llamados BioBricks, o partes biológicas estándar. Estas partes corresponden a fragmentos de ADN que han estado caracterizados y pueden ser combinados para realizar una función determinada en las células donde son implementadas. La competición iGEM facilita el acceso a estas partes proporcionando una base de datos de BioBricks. Además, fomenta que los equipos creen sus propios BioBricks y describan sus características. De esta forma, las agrupaciones estudiantiles contribuyen a expandir la biblioteca digital y los resultados de su proyecto pueden ser utilizados por otras personas interesadas en la biología sintética.
"Los niños serán capaces de diseñar y crear nuevos organismos de manera tan rutinaria como cuando los de mi generación se entretenían con juegos de química. Freeman Dyson, físico y matemático premiado con la medalla Hughes y la medalla Max Planck".
Ante este escenario es interesante saber que cada vez hay más personas científicas que se han lanzado a la gesta titánica de crear vida sintética y como vamos a ver en este artículo, los avances son muy significativos, por lo que debemos prepararnos para asimilar lo que va a suponer para la humanidad contar con los conocimientos y las herramientas necesarias para crear vida de forma artificial, lo cual va a suponer un nuevo salto en nuestra evolución.
Biología sintética para reprogramar células
Un equipo de personas científicas de la Universidad de Cambridge modificaron genéticamente las levaduras con el objetivo de encontrar nuevos medicamentos contra la malaria. Para conseguirlo retiraron unos genes de la levadura y colocaron unos del parásito de la malaria, además de modificar otra muestra con enzimas humanas. El objetivo era identificar qué componentes químicos atacaban los parásitos que causan la enfermedad y no dañan al huésped humano, lo cual permitía descartar los compuestos con posibles efectos secundarios. Las personas científicas han logrado demostrar que el uso de levaduras proporciona una técnica muy económica y resuelve los problemas habituales de la utilización de parásitos vivos. Para demostrar la efectividad de esta nueva herramienta se puso a prueba con el parásito que causa la enfermedad del sueño, ‘trypanosoma brucei’, utilizando la levadura modificada para examinar los compuestos que podrían ser efectivos contra este parásito. Así, de los 36 compuestos, el 60 por ciento pudo matar o inhibir severamente el crecimiento del parásito bajo condiciones normales de laboratorio.
Miranda Wang y Jeanny Yao son dos científicas que contaron con una financiación de 400.000 dólares para la puesta en marcha de la empresa Novoloop (anteriormente BioCellection) con la que buscaban explotar comercialmente las dos patentes fruto de un trabajo de investigación. Utilizando técnicas de biología sintética las científicas desarrollaron una bacteria con capacidad de transformar los ftalatos de los plásticos, que son una toxina peligrosa, en productos finales como dióxido de carbono o agua, lo cual suponía un gran avance para luchar contra la contaminación producida por este material. El objetivo de la empresa es desarrollar estaciones móviles de limpieza para ser instaladas, por ejemplo, en barcos que puedan dedicarse a eliminar los plásticos de los mares. Los barcos podrían contar con 150.000 litros de biodigestores a bordo, cargar los tanques con poliestireno y esperar que los residuos se degraden, todo ello en un proceso que puede durar unas 24 horas.
Un equipo de analistas del MIT, liderado por Christopher Voigt, inventó un lenguaje de programación que permite diseñar bacterias a la carta. El código de este lenguaje de programación se escribe con Cello, basado en Verilog, de forma similar al utilizado para crear chips, programas informáticos y controlar robots, pero en este caso se trata de un lenguaje de programación para bacterias. Gracias a este invento el código se convierte en una secuencia de ADN que, una vez construida, se introduce en una célula para ponerla en marcha. Las bacterias diseñadas hasta el momento llevan a cabo tareas como medir la concentración de oxígeno o glucosa del ambiente, o reconocer diferentes señales y responder a ellas en orden de prioridad. Gracias a este lenguaje de programación para bacterias se reduce significativamente el tiempo necesario para crear células sintéticas, ya que el código programado se convierte automáticamente en ADN. De esta forma, el equipo del MIT ha podido construir el mayor circuito biológico jamás construido, formado por unos 12.000 pares de bases. El lenguaje de programación bacteriano ha sido optimizado para la bacteria Escherichia coli, pero las personas investigadoras involucradas ya trabajan para incluir otros tipos de microorganismos, como pueden ser las levaduras. El objetivo es que el usuario pueda escribir un único programa que luego se traduzca a cada especie para obtener el ADN deseado.
Pero la biología sintética no es la única actividad científica que está permitiendo avanzar en la creación de vida artificial, como vamos a descubrir a continuación, muchas otras personas científicas han trabajado y trabajan con otras estrategias encaminadas al mismo fin.
Creación de órganos artificiales
La empresa Emulate se dedica a la creación de réplicas de órganos humanos de reducido tamaño con el objetivo de ser utilizados para experimentar con químicos y fármacos, lo cual puede ayudar a los médicos y científicos a aprender cómo ciertos alimentos, productos químicos y suplementos dietéticos afectan al cuerpo humano. Por su reducido tamaño son denominados «chips de órganos» y están siendo utilizados en investigaciones por parte de Institutos Nacionales de Salud (NIH), la Agencia de Proyectos de Investigación Avanzada de Defensa (DARPA) y el Centro de Seguridad Alimentaria y Nutrición Aplicada de la FDA. Inicialmente, fueron diseñados para investigar cómo los fármacos funcionan en ciertos órganos, pero ahora también se piensa que pueden ayudar a analizar la seguridad de los alimentos, cosméticos y suplementos dietéticos. Cada chip está desarrollado para simular la fisiología natural de un solo órgano, de forma que ya se ha desarrollado el correspondiente al hígado y se trabaja en los chips de riñón, pulmón e intestino. Los chips son fabricados con un material flexible del polímero que cuenta con unos canales minúsculos, que están revestidos con células humanas vivas del órgano que se estudia. Además, estos dispositivos se pueden colocar en un instrumento de mayor tamaño que permite recrear el ambiente dentro del cuerpo humano. De esta forma las personas científicas serán capaces de inyectar sobre ellos compuestos específicos, como productos químicos de alimentos o productos cosméticos y ver cómo el órgano responde, evitando tener que hacerlo directamente sobre cuerpo humano, y de esta forma ver de manera interconectada cómo una sustancia afecta a múltiples sistemas de órganos en el cuerpo.
Un equipo personas científicas del Instituto Salk de California, dirigidos por Juan Carlos Izpisúa, completaron con éxito el primer experimento para fabricar órganos humanos en cerdos. Sus resultados muestran que podría ser factible crear embriones mezcla de cerdos y humanos, lo cual es un paso fundamental que abre la puerta hacia el futuro de los trasplantes. Este tipo de investigaciones comenzaron en los años setenta, cuando un equipo de personas investigadoras liderado por Nicole Le Douarin creó quimeras entre embriones de pollo y codorniz, para investigar procesos esenciales en el desarrollo embrionario de los vertebrados. También se desarrollaron con éxito de las primeras quimeras de ratones y ratas con el objetivo de poder ser utilizados para hipotéticos trasplantes. Posteriormente, en 2010, el grupo de investigación dirigido por Nakauchi demostró que era posible generar un páncreas de una rata en el interior de un ratón. Al año siguiente, otro equipo de personas científicas logró fabricar un timo de rata en el cuerpo de un ratón. De esta forma, la creación de quimeras interespecies para trasplantes comenzó a ser una realidad, pero el desafío era conseguirlo con células humanas.
Las personas investigadoras que conforman el equipo de Izpisúa trabajan en crear embriones mezcla de cerdos y humanos, inyectando un tipo de células madre inducibles pluripotentes de origen humano en embriones de cerdos, con el objetivo de que los animales incorporen dichas células y puedan hacer que se diferencien correctamente durante el desarrollo embrionario. Sus resultados muestran la primera evidencia de la capacidad de contribución quimérica de células humanas en embriones de cerdo, sin embargo, aún se está lejos de poder fabricar verdaderos órganos humanos en el interior de cerdos. Al analizar las diferentes partes del embrión, detectaron algunas células humanas que, a pesar de implantarse con muy poca eficiencia, sí parecían poder incorporarse a un embrión de una especie diferente durante el desarrollo. Gracias a este trabajo se demuestra que las células madre son capaces de colonizar de forma muy débil, aunque detectable, un embrión anfitrión de cerdo en desarrollo. El desarrollo de estas quimeras servirá para probar medicamentos antes de las pruebas en personas humanas, estudiar el inicio de enfermedades, entender mejor las fases de desarrollo inicial de los embriones humanos y finalmente poder crear en el futuro quimeras de dos especies diferentes como fuente de tejidos y órganos para trasplantes.
Uso de células madre
Un equipo de personas científicas de la Universidad de Cambridge ha logrado crear un embrión artificial de ratón a partir de células madre. Este avance servirá para lograr una mayor comprensión de las etapas más tempranas del desarrollo del embrión y ayudará a explicar los problemas que pueden producirse en esa fase de desarrollo. Intentos previos de hacer crecer estructuras embrionarias usando solo células madre embrionarias habían tenido un éxito limitado, ya que el desarrollo temprano del embrión requiere que los diferentes tipos de células se coordinen estrechamente entre sí. Para lograrlo, las personas investigadoras han utilizado una combinación de células madre embrionarias genéticamente modificadas y de células madre trofoblásticas extraembrionarias, junto con un andamio 3D, conocido como matriz extracelular, sobre el que puedan crecer y han conseguido desarrollar una estructura capaz de ensamblar, cuya arquitectura se parecen mucho al embrión natural. Gracias a este trabajo se ha comprobado que los diferentes tipos de células madre son importantes para el desarrollo y que además trabajan en una verdadera asociación, lo cual permite que el desarrollo y la actividad de los mecanismos biológicos clave se pueda llevar a cabo correctamente. Aunque este embrión artificial se asemeja mucho a uno real, es poco probable que se pueda desarrollar y convertir en un feto sano. Para conseguirlo se necesitaría un tercer tipo de células madre que permitiera el desarrollo del saco vitelino, que proporciona alimento para el embrión y dentro del cual se desarrolla una red de vasos sanguíneos. Además, el sistema no ha sido optimizado para el correcto desarrollo de la placenta.
Con el objetivo de facilitar investigaciones como la que acabamos de comentar, los científicos españoles Miquel Costa y David Horna han desarrollado un biorreactor que permite el cultivo de células madre en serie. El proyecto ha obtenido un millón de euros de inversión por parte de personas inversoras británicas, y ha atraído la atención de la Universidad de Oxford y la empresa farmacéutica Merck. La tecnología desarrollada por Aglaris Cell permite la obtención masiva de cualquier tipo de célula partiendo de otro tipo celular, gracias a la reprogramación celular y a su sistema de cultivo totalmente automatizado. Aglaris Facer 1.0 es el primer biorreactor capaz de ejecutar todas las fases del proceso de cultivo de células de forma completamente automática. Además, presenta una ventaja importante frente al método estándar de cultivo manual, ya que no requiere de la utilización de la tripsina que es tóxica. El procedimiento no requiere de ningún tipo de aditivo ni tampoco de la intervención humana en los pasos de despegado y lavado de las células. En su lugar, el biorreactor integra superficies inteligentes que hacen posible la adhesión y desadhesión de las células en función de cambios en el ambiente. Lo que sí es necesario hacer actualmente de forma manual es la extracción de células de una persona y su posterior inyección en la máquina, donde se cultivan, multiplican y envasan de forma automática.
Replicar funciones vitales de manera artificial
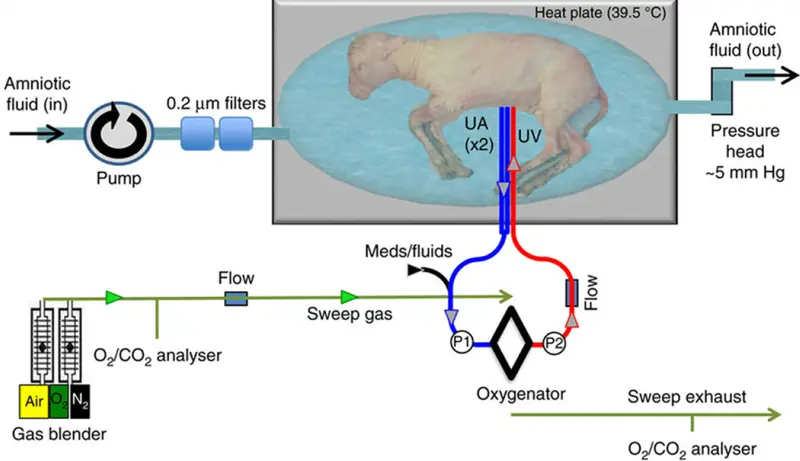
Un equipo de personas investigadoras del hospital de Philadelphia, dirigidos por Alan Flake, ha probado con éxito un dispositivo externo que imita el útero materno y gracias al cual han conseguido mantener con vida a corderos prematuros. Se trata de un primer paso hacia el desarrollo de una matriz artificial que permita mantener a bebés nacidos con menos de 23 semanas de gestación. Este nuevo dispositivo ha permitido mantener con vida durante cuatro semanas a un grupo de corderos ultra prematuros, con un desarrollo equivalente al que tendría un bebé humano de 23-24 semanas de gestación. Hasta ahora, este tipo de dispositivos solo había conseguido mantener con vida unos días a los animales. Igualmente, se trata de la primera vez que el desarrollo de los animales se completa con normalidad. El dispositivo consiste en un sistema cerrado que contiene un fluido que imita el entorno intrauterino y proporciona oxígeno y nutrientes al bebé, mediante un interfaz que imita al cordón umbilical, logrando una circulación estable de sangre y oxígeno durante el periodo de un mes, lo cual ha permitido el desarrollo normal de órganos como los pulmones y el cerebro. Para poder aplicar estos avances en bebés prematuros humanos los científicos tendrían que mejorar considerablemente la conexión umbilical desarrollada.
Un grupo de personas científicas de la Universidad de Northwestern dirigido por Ramille Shah y formado por personas especialistas en el aparato reproductor femenino, reproducción asistida, cirugía, nanotecnología e impresión 3D, ha realizado una investigación para devolver la fertilidad a ratones hembra a las que les habían extirpado los ovarios. Utilizaron la impresión 3D para reproducir la estructura ovárica, para que posteriormente el organismo regenerara el resto del órgano. Para ello imprimieron el andamiaje de unos ovarios artificiales con una gelatina deriva del colágeno, lo implantaron en hembras de ratón esterilizadas y gracias a esa estructura lograron un funcionamiento normal del proceso reproductivo, desde la división celular hasta la ovulación, pasando por la activación hormonal. A los pocos días del implante, minúsculos capilares se extendieron por la gelatina, a las tres semanas ya había vasos sanguíneos irrigando el implante y finalmente los ovarios artificiales activaron el sistema hormonal de las hembras de ratón. El estudio culminó con el apareamiento de una decena de ratones hembra, todas esterilizadas, pero siete de ellas con implantes ováricos, con un resultado en el que 3 de las implantadas se quedaron embarazadas y tuvieron crías. En todos los casos, las madres produjeron leche para alimentarlas.
Un grupo de personas científicas de la Universidad del Sur de California y de la Universidad de Florida han desarrollado en el laboratorio un dispositivo por medio del cual se realiza una sinapsis artificial que puede simular funciones fundamentales del sistema nervioso del ser humano. La capacidad de imitar estas características de la sinapsis biológica en dispositivos semiconductores puede mejorar las funcionalidades y la versatilidad de los sistemas electrónicos neuromórficos, que imitan las estructuras del sistema nervioso, lo cual permitirá a su vez mejorar la capacidad de estos dispositivos, para realizar tareas como el reconocimiento de imágenes, el aprendizaje y la cognición. Las personas involucradas en esta investigación, intentan recrear la sinapsis con el objetivo de desarrollar una inteligencia artificial que pueda imitar mejor las capacidades del cerebro del ser humano.
Robots orgánicos
La empresa de ingeniería Draper, en colaboración con investigadores del Howard Hughes Medical Institute desarrolla un proyecto denominado DragonflEye, en el cual han modificado genéticamente a libélulas con el objetivo de convertirlas en drones. El sistema que han desarrollado está formado por una pequeña mochila con paneles solares para recolectar energía y un sistema integrado de guía y navegación compuesto por herramientas optogenéticas. El sistema DragonflEye es capaz de transmitir órdenes desde la mochila a las neuronas del cerebro de la libélula que determinan la dirección, con la finalidad de controlar el vuelo del insecto a voluntad de un operador. De esta forma han convertido insectos en una especie de drones. Para lograrlo han encontrado una manera de hacer a las libélulas sensibles a la luz, mediante la modificación de genes que se encuentran naturalmente en los ojos, para guiar a los insectos a través de pulsos de luz enviados desde la mochila. Esta tecnología promete aplicaciones complejas, por ejemplo en el ámbito de la seguridad y el espionaje.
La agencia DARPA y la Universidad de Utah trabajan en un proyecto de biónica en el que han implantado un chip en el brazo y una mano robótica a una persona amputada, de forma que cuando esta mueve el brazo, aparece su brazo con una mano virtual adosada en una pantalla. Lo interesante es que cuando la persona realiza acciones como la de abrir una puerta virtual, siente el tacto, de forma biológica y neurológica. En temas similares trabaja el Laboratorio Bensmaia de la Universidad de Chicago, en un proyecto llamado Lifehand 2, que está liderado por Sliman Bensamia y donde han desarrollado un método para trasladar la información desde una mano robótica al cerebro y viceversa. De esta forma cada vez que una persona toca un objeto, una parte del córtex recibe señales sensoriales, por lo que una forma de restaurar la sensibilidad en personas que la han perdido es provocar esa actividad neuronal a través de estimulación eléctrica.
El equipo de personas ingenieras de Suzumori Endo Lab, del Instituto Tecnológico de Tokio, han desarrollado un Robot Musculoesquelético impulsado por músculos multifilamentos. Se trata de músculos formados por múltiples filamentos, con los cuales al realizar pruebas de laboratorio del sistema muscular ha demostrado que es capaz de mover el esqueleto de un androide. A diferencia de los actuadores hidráulicos utilizados más habitualmente en sustitución a los músculos artificiales, este nuevo dispositivo presenta un funcionamiento parecido al de los músculos de personas humanas. Todo ello gracias a que las personas investigadoras involucradas han creado unas piernas para el prototipo que cuentan con el mismo número de fibras musculares que el cuerpo humano. Estas investigaciones abren un mundo de posibilidades en el ámbito del desarrollo de exoesqueletos que puedan ser utilizados por personas con problemas de movilidad o para la creación de robots que simulen las características físicas de los seres humanos.
Nuevos seres orgánicos
200 personas científicas de 10 universidades, liderados por Jef Boeke, del Centro Médico Langone de la Universidad de Nueva York, trabajan en un proyecto llamado Sc2.0 que tiene el objetivo de reemplazar todo el material genético de una célula de levadura con ADN artificial impreso en un laboratorio. El esfuerzo de incorporar cromosomas sintéticos a la levadura de panadería permitirá disponer de una tecnología para imprimir formas de vida mejoradas, o totalmente nuevas, en el laboratorio. Para conseguirlo se han reemplazado cinco de los 16 cromosomas de la levadura con copias artificiales, que han sido modificadas para que el hongo pueda producir fármacos o biocombustibles. Las nuevas copias cromosómicas sintéticas se combinaron con el primer cromosoma que el equipo sintetizó anteriormente, creando una levadura con más de un tercio del genoma de origen artificial. Este proyecto de creación de una levadura sintética forma parte de la iniciativa Genome Project-Write que tiene como objetivo generar un genoma de planta o animal 100% sintético y que comenzó en 2010 cuando un equipo de personas investigadoras del Instituto Craig J. Venter reemplazó el genoma de una bacteria llamada Mycoplasma mycoides por una copia que crearon en el laboratorio. Pero en el caso de las levaduras es mucho más complejo, ya que contienen mucho más ADN que las bacterias, y sus cromosomas contienen entre varios cientos y miles de genes, por lo que las personas responsables serán capaces de remplazar los 16 cromosomas de la levadura con copias artificiales y también generarán un cromosoma extra, el decimoséptimo.
Personas científicas de la Universidad British Columbia de Canadá, liderados por Vitor Pinheiro trabajan en la creación de polímeros sintéticos diferentes al ADN y al ARN, llamados AXN, que pueden almacenar y propagar información, dos de las señas de identidad de la herencia y de la vida. En concreto, se trata de seis polímeros que también cumplen con las leyes de la herencia y, uno de ellos, con la evolución darwiniana, al ser capaz de adaptarse a condiciones cambiantes en el laboratorio de manera análoga a como funciona la evolución. Las moléculas desarrolladas están compuestas por nucleótidos en los que el azúcar desoxirribosa ha sido reemplazado por seis tipos de azúcares distintos, dando lugar a seis moléculas de AXN diferentes. El AXN tiene la capacidad de replicar la información que contiene, al poder unirse de manera complementaria al ADN y al ARN, y también puede sintetizarse a partir de estas cadenas. Además, una de las nuevas moléculas de AXN, llamada AHN, se comporta como el ADN, cuando se encuentra en condiciones cambiantes y puede evolucionar hacia otras formas que se enlazan más específicamente con un objetivo en particular. Por lo tanto, los resultados de esta investigación demuestran que puede haber otras formas de almacenar la información genética distintas a las que conocemos, lo cual abre las puertas a la era de la genética sintética y tiene implicaciones, por ejemplo, en el ámbito de la exobiología.
Personas científicas de la Universidad de Tohoku y el Advanced Institute of Science and Technology de Japón, han fabricado un robot molecular compuesto de biomoléculas, como ADN y proteínas, integrando máquinas moleculares en una membrana celular artificial. El dispositivo está diseñado para iniciar y detener su función de cambio de forma en respuesta a una señal de ADN específica. Esta investigación logró por primera vez que un sistema robótico molecular sea capaz de reconocer señales y controlar su función de cambio de forma, lo cual abre la vía para que los robots moleculares puedan funcionar de una manera similar a los organismos vivos. Un robot molecular es un sistema artificial que se construye integrando máquinas moleculares. Esta máquina robot molecular que se ha desarrollado tiene un tamaño similar a las células humanas y se compone de un actuador molecular, compuesto de proteínas, y un embrague molecular, compuesto de ADN. La forma del cuerpo del robot la determina la membrana celular artificial y puede ser cambiada por el actuador, mientras que la transmisión de la fuerza generada por el actuador puede ser controlada por el embrague molecular. En los experimentos realizados se ha comprobado que la máquina robot molecular puede iniciar y detener el comportamiento de cambio de forma en respuesta a una señal de ADN específica. Los resultados de este estudio podrían conducir a desarrollos tecnológicos que ayuden a resolver importantes problemas médicos, como una máquina de tratamiento para células vivas de cultivo, o una máquina de monitoreo para controlar la contaminación ambiental.
Las personas científicas del Instituto de Investigación Scripps liderados por Floyd Romesberg, afirman haber fabricado el organismo semisintético estable más parecido a la vida, un avance que podría tener importantes implicaciones para la medicina e incluso preparar el terreno para la creación de nuevas formas de vida. En 2014 estos científicos ampliaron el código genético de cuatro a seis letras, agregando dos bases sintéticas llamadas X e Y al ADN de la bacteria Escherichia coli. Sin embargo, el organismo semisintético resultante crecía con lentitud y no podía mantener el par de base sintético de forma indefinida en su código a medida que se dividía. Ahora los investigadores han optimizado una herramienta llamada transportador nucleótido, que ha permitido al organismo semisintético crecer y dividirse, a la vez que conserva la X y la Y añadidas. Aunque por el momento las aplicaciones reales de este organismo semisintético no están claras, este trabajo podría ser utilizado en el futuro para crear nuevas funciones en los organismos unicelulares que desempeñan papeles importantes en el descubrimiento de fármacos.
Seres digitales y vida artificial
"Los virus de computadoras deberían ser considerados como vida. Pienso que esto dice algo acerca de la naturaleza humana, que la única forma de vida que hemos creado es puramente destructiva. Hemos creado una forma de vida a nuestra imagen y semejanza. Stephen Hawking".
El científico Tim Busbice logró en 2014 reproducir digitalmente las 302 neuronas, 6.418 sinapsis y los 95 músculos inervadores, que conforman el cerebro del gusano Caenorhabditis elegans, el cual también fue el primer organismo multicelular en ser secuenciado genéticamente por completo. Para replicar su cerebro de manera digital fueron necesarios 302 programas, uno por cada neurona, conectados todos ellos entre sí, de una manera similar a la llamada comunicación sináptica, para posteriormente conectar el sistema a un robot, originalmente un Lego Mindstorms EV3 Robot, a través del cual pudo interactuar libremente con el entorno. Al encender el robot, este se movía tras captar un sonido, como hace de manera natural el gusano biológico, buscando encontrar trazas de alimento. Cuando el robot se mueve y se encuentra con un obstáculo, busca sortearlo, pero no por haber sido programado de forma previa, sino como resultado de su propia interacción y aprendizaje. Este proyecto ha sido desarrollado en formato open source a través de la iniciativa OpenWorm y posteriormente ha evolucionado para convertirse en una empresa llamada Connectome Engine que se dedica a la creación de seres inorgánicos.
Un equipo de personas científicas de la Universidad de Trento han creado células artificiales capaces de comunicarse con bacterias y hacerlas creer que son reales. Para conseguirlo han diseñado unas estructuras a imitación de las células, con instrucciones de ADN que podían usarse para construir RNA, que en respuestas a estímulos exteriores pueden producir proteínas específicas, solo en presencia de una molécula de ciertas bacterias. Cuando se sitúa a estas células artificiales cerca de algunas bacterias, estas reaccionan produciendo proteínas. Al comprobar que esto funcionaba, las personas científicas han ido más allá, desarrollando en las células artificiales la habilidad de producir la molécula que las bacterias segregan. De esta forma se ha logrado que células artificiales y bacterias puedan comunicarse entre sí. Las personas científicas piensan que las células artificiales podrían servir en el futuro para interferir en infecciones causadas por bacterias, lo cual podría desembocar en un método que permita frenar determinadas enfermedades.
Hasta aquí hemos llegado con este repaso a las iniciativas de investigación que se están desarrollando a nivel mundial en relación con la creación de vida artificial. A este respecto no hemos querido hablar sobre cómo todas estas tecnologías se podrían utilizar sobre el ser humano en el ámbito de lo que se ha denominado como Eugenesia, lo cual desde luego tiene unas implicaciones éticas que la sociedad debe conocer y que deposita en las personas científicas una gran responsabilidad, al respecto de cómo todos estos avances pueden influir en el futuro de la humanidad. Porque lo que está claro es que nos encontramos en un momento clave en la evolución humana, que va más allá de la selección natural y sitúa a las personas como protagonistas de un futuro en el que la unión entre la biología con la tecnología y la inteligencia artificial, nos situará en escenarios para los que nuestra mente aún no está preparada.
Nuestras últimas novedades
¿Te interesa saber cómo nos adaptamos constantemente a la nueva frontera digital?

Tech Insight
13 de enero de 2025
Cómo acercar tu aplicación a todas las personas

Insight
10 de diciembre de 2024
Tecnologías rompedoras hoy, que redibujarán el mapa de la innovación en 2025

Insight
4 de diciembre de 2024
Un Viaje de Innovación, Superación y Magia

Insight
3 de diciembre de 2024
Desarrollo sostenible: Minimizando la huella digital y optimizando el consumo
